Вероятно, все вы видели периодическую таблицу элементов. Возможно, что она и по сей день преследует вас в ваших снах, а может быть, она пока для вас всего лишь визуальный фон, украшающий стенку школьного класса. Однако в этой, казалось бы, случайной коллекции клеток кроется значительно больше, чем это кажется на первый взгляд.
Периодическая таблица (или ПТ, как мы будем периодически называть её в этой статье), а также те элементы, которые входят в неё, обладают чертами, о которых вы, возможно, никогда не догадывались. Вот десять фактов, начиная от создания таблицы и до внесения в неё последних элементов, которые большинству людей не известны.
10. Менделееву помогали
Периодическая таблица стала использоваться, начиная с 1869 года, когда она была составлена заросшим густой бородой Димитрием Менделеевым. Большинство людей думает, что Менделеев был единственным, кто работал над этой таблицей, и благодаря этому он стал самым гениальным химиком столетия. Однако его усилиям помогали несколько европейских учёных, которые внесли важный вклад в завершение этого колоссального набора элементов.
Менделеев широко известен как отец периодической таблицы, но, когда он её составлял, ещё не все элементы таблицы были уже открыты. Как такое стало возможно? Учёные славятся своим безумием…
9. Последние добавленные элементы

Верьте или нет, периодическая таблица не сильно менялась с 1950-х годов. Однако 2 декабря 2016 года было добавлено сразу четыре новых элемента: нихоний (элемент №113), московий (элемент №115), тенессин (элемент №117) и оганесон (элемент №118). Эти новые элементы получили свои названия только в июне 2016 года, так как потребовалась пятимесячная экспертиза, прежде чем их официально добавили в ПТ.
Три элемента получили свои названия в честь городов или государств, в которых их удалось получить, а оганесон был назван в честь российского физика-ядерщика Юрия Оганесяна за его вклад в получение этого элемента.
8. Какой буквы нет в таблице?

В латинском алфавите есть 26 букв, и каждая из них важна. Однако Менделеев решил этого не замечать. Взгляните на таблицу и скажите, какой букве не повезло? Подсказка: ищите по порядку и загибайте при этом пальцы после каждой найденной буквы. В итоге вы найдёте «пропавшую» букву (если у вас на руках присутствуют все десять пальцев). Догадались? Это буква под номером 10, буква «J».
Говорят, что «единица» - это цифра одиноких. Так, может, стоило бы назвать букву «J» буквой одиноких? Но вот забавный факт: большинство мальчиков, родившихся в США в 2000 году, получили имена, начинавшиеся с этой буквы. Таким образом, эта буква не осталась без должного внимания.
7. Синтезированные элементы

Как вы, возможно, уже знаете, на сегодняшний день в периодической таблице присутствует 118 элементов. Можете ли вы догадаться, сколько элементов из этих 118 были получены лабораторным путём? Из всего общего списка в природных условиях можно найти лишь 90 элементов.
Вам кажется, что 28 искусственно созданных элементов - это много? Ну, просто поверьте на слово. Их синтезируют, начиная с 1937 года, и учёные продолжают это делать и сейчас. Все эти элементы вы можете найти в таблице. Посмотрите на элементы с 95 по 118, все эти элементы отсутствуют на нашей планете и были синтезированы в лабораториях. То же касается и элементов под номерами 43, 61, 85 и 87.
6. 137-й элемент

В середине 20-го века известный учёный по имени Ричард Фейнман сделал довольно громкое заявление, которое повергло в изумление весь научный мир нашей планеты. По его словам, если мы когда-нибудь обнаружим 137-й элемент, то мы не сможем определить количество в нём протонов и нейтронов. Число 1/137 примечательно тем, что это значение константы тонкой структуры, которая описывает вероятность поглощения или излучения электроном фотона. Теоретически элемент №137 должен иметь 137 электронов и 100-процентную вероятность поглощения фотона. Его электроны будут вращаться со скоростью света. Ещё более невероятно, что электроны элемента 139, чтобы существовать, должны вращаться быстрее, чем скорость света.
Вы ещё не устали от физики? Возможно, вам будет интересно узнать, что число 137 объединяет три важнейших области физики: теорию о скорости света, квантовую механику и электромагнетизм. С начала 1900-х годов физики предполагают, что цифра 137 может быть основой Великой единой теории, в которую войдут все три вышеуказанных области. По общему признанию, это звучит так же невероятно, как легенды о НЛО и о Бермудском треугольнике.
5. Что можно сказать о названиях?

Почти все названия элементов имеют какой-то смысл, хотя он и не сразу понятен. Названия новым элементам даются не произвольно. Я бы назвал элемент просто первым пришедшим мне в голову словом. Например, «керфлумп». По-моему, неплохо.
Как правило, названия элементов относятся к одной из пяти основных категорий. Первая - это имена известных учёных, классический вариант - эйнштейний. Кроме того, элементы могут получить свои имена в зависимости от тех мест, где они были впервые зарегистрированы, например, германий, америций, галлий и т. д. В качестве дополнительной опции используются названия планет. Элемент уран был впервые обнаружен вскоре после того, как была открыта планета Уран. Элементы могут носить имена, связанные с мифологией, например, существует титан, названный так в честь древнегреческих титанов, и торий, названный по имени скандинавского бога-громовержца (или звёздного «мстителя», в зависимости от того, что вы предпочитаете).
И, наконец, есть названия, описывающие свойства элементов. Аргон происходит от греческого слова «аргос», что означает «ленивый» или «медленный». Из названия следует предположение, что этот газ не отличается активностью. Бром - это ещё один элемент, название которого происходит от греческого слова. «Бромос» означает «зловоние», и это довольно точно описывает запах брома.
4. Было ли создание таблицы «озарением»

Если вы любите карточные игры, то этот факт для вас. Менделееву требовалось каким-то образом упорядочить все элементы и найти систему для этого. Естественно, что для создания таблицы по категориям он обратился к пасьянсу (ну, а к чему же ещё?) Менделеев записал атомный вес каждого элемента на отдельной карточке, а затем приступил к раскладке своего передового пасьянса. Он укладывал элементы в соответствии с их специфическими свойствами, а затем упорядочивал их в каждом столбце в соответствии с их атомным весом.
Многие не могут сложить и обычный пасьянс, так что этот пасьянс впечатляет. Что будет дальше? Наверное, кто-нибудь с помощью шахмат сделает переворот в астрофизике или создаст ракету, способную долететь до окраин галактики. Представляется, что в этом не будет ничего необычного, если учесть, что Менделеев сумел получить такой гениальный результат всего лишь с помощью колоды обычных игральных карт.
3. Невезучие инертные газы

Помните, как мы классифицировали аргон как самый «ленивый» и «медленный» элемент в истории нашей вселенной? Похоже, что Менделеевым овладели такие же чувства. Когда в 1894 году впервые удалось получить чистый аргон, он не вписывался ни в один из столбцов таблицы, поэтому, вместо того чтобы заняться поисками решения, учёный решил просто отрицать его существование.
Ещё более поразительно, что аргон был не единственным элементом, который изначально постигла эта судьба. Помимо аргона, без классификации остались ещё пять других элементов. Это коснулось радона, неона, криптона, гелия и ксенона - и все отрицали их существование просто потому, что Менделеев не смог найти для них места в таблице. После нескольких лет перегруппировки и переклассификации этим элементам (названных инертными газами) всё-таки посчастливилось присоединиться к достойному клубу признанных реально существующими.
2. Атомная любовь

Совет для всех тех, кто считает себя романтиком. Возьмите бумажную копию периодической таблицы и вырежьте из неё все сложные и относительно ненужные средние столбцы так, чтобы у вас осталось 8 колонок (вы получите «короткую» форму таблицы). Сложите её посредине IV группы - и вы узнаете, какие элементы могут образовывать соединения друг с другом.
Элементы, которые «целуются» при складывании, способны образовывать стабильные соединения. Эти элементы имеют комплементарные электронные структуры, и они будут сочетаться друг с другом. И, если это не настоящая любовь, как у Ромео с Джульеттой или у Шрека с Фионой - тогда я не знаю, что такое любовь.
1. Углерод рулит

Углерод пытается быть в центре игры. Вы думаете, что всё знаете об углероде, но это не так, он занимает намного более важное место, чем вы это себе представляете. Знаете ли вы, что он присутствует более чем в половине всех известных соединений? И как насчёт того факта, что 20 процентов веса всех живых организмов приходится на углерод? Это действительно странно, но приготовьтесь: каждый атом углерода в вашем теле был когда-то частью фракции углекислого газа в атмосфере. Углерод является не только суперэлементом нашей планеты, он четвёртый по численности элемент во всей Вселенной.
Если периодическую таблицу сравнить с вечеринкой, то углерод - её главный ведущий. И кажется, что он единственный знает, как нужно всё правильно организовать. Ну и, помимо прочего, это основной элемент всех бриллиантов, так что при всей своей назойливости он ещё и блестит!
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Построение периодической таблицы химических элементов Менделеева отвечает характерным периодам теории чисел и ортогональных базисов. Дополнение матриц Адамара матрицами четных и нечетных порядков создает структурный базис вложенных матричных элементов: матриц первого (Odin), второго (Euler), третьего (Mersenne), четвертого (Hadamard) и пятого (Fermat) порядков.
Несложно заметить, что порядкам 4k матриц Адамара соответствуют инертные элементы с атомной массой, кратной четырем: гелий 4, неон 20, аргон 40 (39.948) и т.п., но также и основы жизни и цифровой техники: углерод 12, кислород 16, кремний 28, германий 72.
Такое впечатление, что с матрицами Мерсенна порядков 4k –1, напротив, связано все активное, ядовитое, разрушительное и разъедающее. Но это также радиоактивные элементы – источники энергии, и свинец 207 (конечный продукт, ядовитые соли). Фтор, это, конечно, 19. Порядкам матриц Мерсенна отвечает последовательность радиоактивных элементов, называемая рядом актиния: уран 235, плутоний 239 (изотоп, который является более мощным источником атомной энергии, чем уран) и т.п. Это также щелочные металлы литий 7, натрий 23 и калий 39.

Галлий – атомный вес 68
Порядкам 4k –2 матриц Эйлера (сдвоенный Мерсенн) соответствует азот 14 (основа атмосферы). Поваренная соль образована двумя "мерсенноподобными" атомами натрия 23 и хлора 35, вместе это сочетание характерно, как раз, для матриц Эйлера. Более массивный хлор с весом 35.4 немногим не добирает до адамаровой размерности 36. Кристаллы поваренной соли: куб (! т.е. характер смирный, адамаров) и октаэдр (более вызывающий, это несомненный Эйлер).
В атомной физике переход железо 56 – никель 59, это рубеж между элементами, дающими энергию при синтезе более крупного ядра (водородная бомба) и распаде (урановая). Порядок 58 знаменит тем, что для него нет не только аналогов матриц Адамара в виде матриц Белевича с нулями на диагонали, для него нет и многих взвешенных матриц – ближайшая ортогональная W(58,53) имеет 5 нулей в каждом столбце и строке (глубокий разрыв).
В ряду, соответствующем матрицам Ферма и их замещениям порядков 4k +1, стоит волею судьбы фермий 257. Ничего не скажешь, точное попадание. Здесь же золото 197. Медь 64 (63.547) и серебро 108 (107.868), символы электроники, недотягивают, как видно, до золота и соответствуют более скромным матрицам Адамара. Медь, с ее недалеко ушедшим от 63 атомным весом, химически активна – ее зеленые окислы хорошо известны.
Кристаллы бора под сильным увеличением
С золотым сечением связан бор – атомная масса среди всех прочих элементов наиболее близка к 10 (точнее 10.8, близость атомного веса к нечетным числам тоже сказывается). Бор – достаточно сложный элемент. Бор играет запутанную роль в истории самой жизни. Строение каркаса в его структурах гораздо сложнее, чем в алмазе. Уникальный тип химической связи, которая позволяет бору поглощать любую примесь, очень плохо изучен, хотя за исследования, связанные с ним, большое количество ученых уже получили Нобелевские премии. Форма кристалла бора – икосаэдр, пять треугольников образуют вершину.
Загадка Платины. Пятый элемент, это, без сомнения, благородные металлы, такие, как золото. Надстройка над адамаровой размерностью 4k , на 1 большие.

Стабильный изотоп уран 238
Вспомним, все же, что числа Ферма встречаются редко (ближайшее – 257). Кристаллы самородного золота имеют форму, близкую к кубу, но и пентаграмма просверкивает. Его ближайший сосед, платина, благородный металл, отстоит от золота 197 по атомному весу меньше, чем на 4. Платина имеет атомный вес не 193, а несколько повышенный, 194 (порядок матриц Эйлера). Мелочь, но это переносит ее в стан несколько более агрессивных элементов. Стоит вспомнить, в связи, что при ее инертности (растворяется, разве, в царской водке), платину используют как активный катализатор химических процессов.
Губчатая платина при комнатной температуре воспламеняет водород. Характер у платины вовсе не мирный, смирнее себя ведет иридий 192 (смесь изотопов 191 и 193). Это, скорее, медь, но с весом и характером золота.
Между неоном 20 и натрием 23 нет элемента с атомным весом 22. Конечно, атомные веса – интегральная характеристика. Но среди изотопов, в свою очередь, тоже наблюдается любопытная корреляция свойств со свойствами чисел и соответствующих им матриц ортогональных базисов. В качестве ядерного топлива наибольшее применение имеет изотоп уран 235 (порядок матриц Мерсенна), в котором возможна самоподдерживающаяся цепная ядерная реакция. В природе этот элемент распространен стабильной форме уран 238 (порядок матриц Эйлера). Элемент с атомным весом 13 отсутствует. Что касается хаоса, то ограниченное количество устойчивых элементов таблицы Менделеева и сложность нахождения уровневых матриц высоких порядков ввиду замеченного у матриц тринадцатого порядка барьера коррелируют.
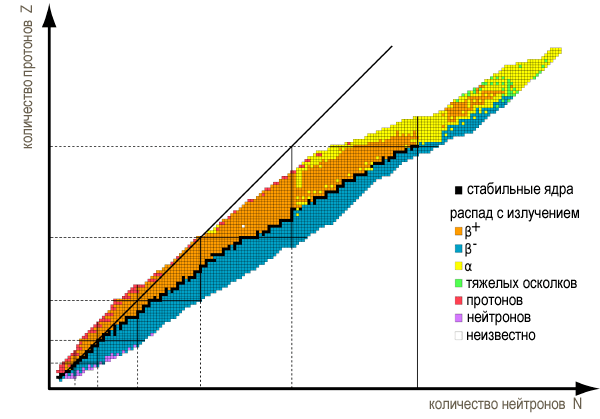
Изотопы химических элементов, островок стабильности
Периодический закон Д.И. Менделеева и периодическая система химических элементов имеет большое значение в развитии химии. Окунемся в 1871 год, когда профессор химии Д.И. Менделеев, методом многочисленных проб и ошибок, пришел к выводу, что «… свойства элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса». Периодичность изменения свойств элементов возникает вследствие периодического повторения электронной конфигурации внешнего электронного слоя с увеличением заряда ядра.
Современная формулировка периодического закона
такова:
«свойства химических элементов (т.е. свойства и форма образуемых ими соединений) находятся в периодической зависимости от заряда ядра атомов химических элементов».
Преподавая химию, Менделеев понимал, что запоминание индивидуальных свойств каждого элемента, вызывает у студентов трудности. Он стал искать пути создания системного метода, чтобы облегчить запоминание свойств элементов. В результате появилась естественная таблица , позже она стала называться периодической .
Наша современная таблица очень похожа на менделеевскую. Рассмотрим ее подробнее.
Таблица Менделеева
Периодическая таблица Менделеева состоит из 8 групп и 7 периодов.
Вертикальные столбцы таблицы называют группами . Элементы, внутри каждой группы, обладают сходными химическими и физическими свойствами. Это объясняется тем, что элементы одной группы имеют сходные электронные конфигурации внешнего слоя, число электронов на котором равно номеру группы. При этом группа разделяется на главные и побочные подгруппы .
В Главные подгруппы входят элементы, у которых валентные электроны располагаются на внешних ns- и np- подуровнях. В Побочные подгруппы входят элементы, у которых валентные электроны располагаются на внешнем ns- подуровне и внутреннем (n — 1) d- подуровне (или (n — 2) f- подуровне).
Все элементы в периодической таблице , в зависимости от того, на каком подуровне (s-, p-, d- или f-) находятся валентные электроны классифицируются на: s- элементы (элементы главной подгруппы I и II групп), p- элементы (элементы главных подгрупп III — VII групп), d- элементы (элементы побочных подгрупп), f- элементы (лантаноиды, актиноиды).
Высшая валентность элемента (за исключением O, F, элементов подгруппы меди и восьмой группы) равна номеру группы, в которой он находится.
Для элементов главных и побочных подгрупп одинаковыми являются формулы высших оксидов (и их гидратов). В главных подгруппах состав водородных соединений являются одинаковыми, для элементов, находящихся в этой группе. Твердые гидриды образуют элементы главных подгрупп I — III групп, а IV — VII групп образуют а газообразные водородные соединения. Водородные соединения типа ЭН 4 – нейтральнее соединения, ЭН 3 – основания, Н 2 Э и НЭ — кислоты.
Горизонтальные ряды таблицы называют периодами . Элементы в периодах отличаются между собой, но общее у них то, что последние электроны находятся на одном энергетическом уровне (главное квантовое число n — одинаково).
Первый период отличается от других тем, что там находятся всего 2 элемента: водород H и гелий He.
Во втором периоде находятся 8 элементов (Li - Ne). Литий Li – щелочной металл начинает период, а замыкает его благородный газ неон Ne.
В третьем периоде, также как и во втором находятся 8 элементов (Na - Ar). Начинает период щелочной металл натрий Na, а замыкает его благородный газ аргон Ar.
В четвёртом периоде находятся 18 элементов (K - Kr) – Менделеев его обозначил как первый большой период. Начинается он также с щелочного металла Калий, а заканчивается инертным газом криптон Kr. В состав больших периодов входят переходные элементы (Sc - Zn) — d- элементы.
В пятом периоде, аналогично четвертому находятся 18 элементов (Rb - Xe) и структура его сходна с четвёртым. Начинается он также с щелочного металла рубидий Rb, а заканчивается инертным газом ксенон Xe. В состав больших периодов входят переходные элементы (Y - Cd) — d- элементы.
Шестой период состоит из 32 элементов (Cs - Rn). Кроме 10 d -элементов (La, Hf - Hg) в нем находится ряд из 14 f -элементов(лантаноиды)- Ce — Lu
Седьмой период не закончен. Он начинается с Франций Fr, можно предположить, что он будет содержать, также как и шестой период, 32 элемента, которые уже найдены (до элемента с Z = 118).
Интерактивная таблица Менделеева
Если посмотреть на периодическую таблицу Менделеева и провести воображаемую черту, начинающуюся у бора и заканчивающуюся между полонием и астатом, то все металлы будут находиться слева от черты, а неметаллы – справа. Элементы, непосредственно прилегающие к этой линии будут обладать свойствами как металлов, так и неметаллов. Их называют металлоидами или полуметаллами. Это бор, кремний, германий, мышьяк, сурьма, теллур и полоний.
Периодический закон
Менделеев дал следующую формулировку Периодического закона: «свойства простых тел, а также формы и свойства соединений элементов, а потому и свойства образуемых ими простых и сложных тел, стоят в периодической зависимости от их атомного веса».
Существует четыре основных периодических закономерности:
Правило октета
утверждает, что все элементы стремятся приобрести или потерять электрон, чтобы иметь восьмиэлектронную конфигурацию ближайшего благородного газа. Т.к. внешние s- и p-орбитали благородных газов полностью заполнены, то они являются самыми стабильными элементами.
Энергия ионизации
– это количество энергии, необходимое для отрыва электрона от атома. Согласно правилу октета, при движении по периодической таблице слева направо для отрыва электрона требуется больше энергии. Поэтому элементы с левой стороны таблицы стремятся потерять электрон, а с правой стороны – его приобрести. Самая высокая энергия ионизации у инертных газов. Энергия ионизации уменьшается при движении вниз по группе, т.к. у электронов низких энергетических уровней есть способность отталкивать электроны с более высоких энергетических уровней. Это явление названо эффектом экранирования
. Благодаря этому эффекту внешние электроны мене прочно связаны с ядром. Двигаясь по периоду энергия ионизации плавно увеличивается слева направо.

Сродство к электрону – изменение энергии при приобретении дополнительного электрона атомом вещества в газообразном состоянии. При движении по группе вниз сродство к электрону становится менее отрицательным вследствие эффекта экранирования.

Электроотрицательность — мера того, насколько сильно стремится притягивать к себе электроны связанного с ним другого атома. Электроотрицательность увеличивается при движении в периодической таблице слева направо и снизу вверх. При этом надо помнить, что благородные газы не имеют электроотрицательности. Таким образом, самый электроотрицательный элемент – фтор.

На основании этих понятий, рассмотрим как меняются свойства атомов и их соединений в таблице Менделеева.
Итак, в периодической зависимости находятся такие свойства атома, которые связанны с его электронной конфигурацией: атомный радиус, энергия ионизации, электроотрицательность.
Рассмотрим изменение свойств атомов и их соединений в зависимости от положения в периодической системе химических элементов .
Неметалличность атома увеличивается при движении в периодической таблице слева направо и снизу вверх . В связи с этим основные свойства оксидов уменьшаются, а кислотные свойства увеличиваются в том же порядке — при движении слева направо и снизу вверх. При этом кислотные свойства оксидов тем сильнее, чем больше степень окисления образующего его элемента
По периоду слева направо основные свойства гидроксидов ослабевают,по главным подгруппам сверху вниз сила оснований увеличивается. При этом, если металл может образовать несколько гидроксидов, то с увеличением степени окисления металла, основные свойства гидроксидов ослабевают.
По периоду слева направо увеличивается сила кислородосодержащих кислот. При движении сверху вниз в пределах одной группы сила кислородосодержащих кислот уменьшается. При этом сила кислоты увеличивается с увеличением степени окисления образующего кислоту элемента.
По периоду слева направо увеличивается сила бескислородных кислот. При движении сверху вниз в пределах одной группы сила бескислородных кислот увеличивается.
Категории ,Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
Периодическая система химических элементов Д. И. Менделеева
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.
Периодический закон
Существуют две формулировки периодического закона химических элементов: классическая и современная.
Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов .
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера) .
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.

Группы и периоды Периодической системы
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом - 32, а в седьмом (пока незавершенном) - 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
Свойства таблицы Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R 2 O, RO, R 2 O 3 , RO 2 , R 2 O 5 , RO 3 , R 2 O 7 , RO 4 , где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R 2 O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO 2 , R 2 O 5 , RO 3 , R 2 O 7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH 4 , RH 3 , RH 2 , RH.
Соединения RH 4 имеют нейтральный характер; RH 3 - слабоосновный; RH 2 - слабокислый; RH - сильнокислый характер.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.

Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы - мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
Показать / Скрыть текст
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды - это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
Показать / Скрыть текст
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газах все электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
Показать / Скрыть текст
Переходные металлы
Переходные металлы занимают группы 3-12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
Показать / Скрыть текст
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13-16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
Показать / Скрыть текст
Постпереходными металлами
Элементы, называемые постпереходными металлами , относятся к группам 13-15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Периодическая система химических элементов - это классификация химических элементов, созданная Д. И. Менделеевым на основе открытого им в 1869 г. периодического закона.
Д. И. Менделеев
Согласно современной формулировке этого закона, в непрерывном ряду элементов, расположенных в порядке возрастания величины положительного заряда ядер их атомов, периодически повторяются элементы со сходными свойствами.
Периодическая система химических элементов, представленная в виде таблицы, состоит из периодов, рядов и групп.
В начале каждого периода (за исключением первого) находится элементе ярко выраженными металлическими свойствами (щелочной металл).

Условные обозначения к цветной таблице: 1 - химический знак элемента; 2 - название; 3 - атомная масса (атомный вес); 4 - порядковый номер; 5 - распределение электронов по слоям.
По мере возрастания порядкового номера элемента, равного величине положительного заряда ядра его атома, постепенно ослабевают металлические и нарастают неметаллические свойства. Предпоследним элементом в каждом периоде является элемент с ярко выраженными неметаллическими свойствами (), а последним - инертный газ. В I периоде находятся 2 элемента, во II и III - по 8 элементов, в IV и V - по 18, в VI - 32 и в VII (не завершенном периоде) - 17 элементов.
Первые три периода называют малыми периодами, каждый из них состоит из одного горизонтального ряда; остальные - большими периодами, каждый из которых (исключая VII период) состоит из двух горизонтальных рядов - четного (верхнего) и нечетного (нижнего). В четных рядах больших периодов находятся только металлы. Свойства элементов в этих рядах с возрастанием порядкового номера изменяются слабо. Свойства элементов в нечетных рядах больших периодов меняются. В VI периоде за лантаном следуют 14 элементов, весьма сходных по химическим свойствам. Эти элементы, называемые лантаноидами, приведены отдельно под основной таблицей. Аналогично представлены в таблице и актиноиды - элементы, следующие за актинием.

В таблице имеется девять вертикальных групп. Номер группы, за редким исключением, равен высшей положительной валентности элементов данной группы. Каждая группа, исключая нулевую и восьмую, подразделяется на подгруппы. - главную (расположена правее) и побочную. В главных подгруппах с увеличением порядкового номера усиливаются металлические и ослабевают неметаллические свойства элементов.
Таким образом, химические и ряд физических свойств элементов определяются местом, которое занимает данный элемент в периодической системе.
Биогенные элементы, т. е. элементы, входящие в состав организмов и выполняющие в нем определенную биологическую роль, занимают верхнюю часть таблицы Менделеева. В голубой цвет окрашены клетки, занимаемые элементами, составляющими основную массу (более 99%) живого вещества, в розовый цвет - клетки, занимаемые микроэлементами (см.).
Периодическая система химических элементов является крупнейшим достижением современного естествознания и ярким выражением наиболее общих диалектических законов природы.
См. также , Атомный вес.
Периодическая система химических элементов - естественная классификация химических элементов, созданная Д. И. Менделеевым на основе открытого им в 1869 г. периодического закона.
В первоначальной формулировке периодический закон Д. И. Менделеева утверждал: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины атомных весов элементов. В дальнейшем с развитием учения о строении атома было показано, что более точной характеристикой каждого элемента является не атомный вес (см.), а величина положительного заряда ядра атома элемента, равная порядковому (атомному) номеру этого элемента в периодической системе Д. И. Менделеева. Число положительных зарядов ядра атома равно числу электронов, окружающих ядро атома, поскольку атомы в целом электронейтральны. В свете этих данных периодический закон формулируется так: свойства химических элементов, а также формы и свойства их соединений находятся в периодической зависимости от величины положительного заряда ядер их атомов. Это значит, что в непрерывном ряду элементов, расположенных в порядке возрастания положительных зарядов ядер их атомов, будут периодически повторяться элементы со сходными свойствами.
Табличная форма периодической системы химических элементов представлена в ее современном виде. Она состоит из периодов, рядов и групп. Период представляет последовательный горизонтальный ряд элементов, расположенных в порядке возрастания положительного заряда ядер их атомов.
В начале каждого периода (за исключением первого) находится элемент с ярко выраженными металлическими свойствами (щелочной металл). Затем по мере увеличения порядкового номера постепенно ослабевают металлические и нарастают неметаллические свойства элементов. Предпоследним элементом в каждом периоде является элемент с ярко выраженными неметаллическими свойствами (галоген), а последним - инертный газ. I период состоит из двух элементов, роль щелочного металла и галогена здесь одновременно выполняет водород. II и III периоды включают по 8 элементов, названных Менделеевым типическими. IV и V периоды насчитывают по 18 элементов, VI-32. VII период еще не завершен и пополняется искусственно создаваемыми элементами; в настоящее время в этом периоде насчитывается 17 элементов. I, II и III периоды называют малыми, каждый из них состоит из одного горизонтального ряда, IV-VII- большими: они (за исключением VII) включают два горизонтальных ряда - четный (верхний) и нечетный (нижний). В четных рядах больших периодов находятся только металлы, и изменение свойств элементов в ряду слева направо выражено слабо.
В нечетных рядах больших периодов свойства элементов в ряду изменяются так же, как свойства типических элементов. В четном ряду VI периода после лантана следует 14 элементов [называемых лантанидами (см.), лантаноидами, редкоземельными элементами], сходных по химическим свойствам с лантаном и между собой. Перечень их приводится отдельно под таблицей.
Отдельно выписаны и приведены под таблицей элементы, следующие за актинием- актиниды (актиноиды).
В периодической системе химических элементов по вертикалям расположено девять групп. Номер группы равен высшей положительной валентности (см.) элементов этой группы. Исключение составляют фтор (бывает только отрицательно одновалентным) и бром (не бывает семивалентным); кроме того, медь, серебро, золото могут проявлять валентность больше +1 (Cu-1 и 2, Ag и Au-1 и 3), а из элементов VIII группы валентностью +8 обладают только осмий и рутений. Каждая группа, за исключением восьмой и нулевой, делится на две подгруппы: главную (расположена правее) и побочную. В главные подгруппы входят типические элементы и элементы больших периодов, в побочные - только элементы больших периодов и притом металлы.
По химическим свойствам элементы каждой подгруппы данной группы значительно отличаются друг от друга и только высшая положительная валентность одинакова для всех элементов данной группы. В главных подгруппах сверху вниз усиливаются металлические свойства элементов и ослабевают неметаллические (так, франций является элементом с наиболее ярко выраженными металлическими свойствами, а фтор - неметаллическими). Таким образом, место элемента в периодической системе Менделеева (порядковый номер) определяет его свойства, которые представляют собой среднее из свойств соседних элементов по вертикали и горизонтали.
Некоторые группы элементов носят особые названия. Так, элементы главных подгрупп I группы называют щелочными металлами, II группы - щелочноземельными металлами, VII группы - галогенами, элементы, расположенные за ураном,- трансурановыми. Элементы, которые входят в состав организмов, принимают участие в процессах обмена веществ и обладают явно выраженной биологической ролью, называют биогенными элементами. Все они занимают верхнюю часть таблицы Д. И. Менделеева. Это в первую очередь О, С, Н, N, Са, Р, К, S, Na, Cl, Mg и Fe, составляющие основную массу живого вещества (более 99%). Места, занимаемые этими элементами в периодической системе, окрашены в светло-голубой цвет. Биогенные элементы, которых в организме очень мало (от 10 -3 до 10 -14 %), называют микроэлементами (см.). В клетках периодической системы, окрашенных в желтый цвет, помещены микроэлементы, жизненно важное значение которых для человека доказано.
Согласно теории строения атомов (см. Атом) химические свойства элементов зависят в основном от числа электронов на внешней электронной оболочке. Периодическое изменение свойств элементов с увеличением положительного заряда атомных ядер объясняется периодическим повторением строения наружной электронной оболочки (энергетического уровня) атомов.
В малых периодах с увеличением положительного заряда ядра возрастает число электронов на внешней оболочке от 1 до 2 в I периоде и от 1 до 8 во II и III периодах. Отсюда изменение свойств элементов в периоде от щелочного металла до инертного газа. Внешняя электронная оболочка, содержащая 8 электронов, является завершенной и энергетически устойчивой (элементы нулевой группы химически инертны).
В больших периодах в четных рядах с ростом положительного заряда ядер число электронов на внешней оболочке остается постоянным (1 или 2) и идет заполнение электронами второй снаружи оболочки. Отсюда медленное изменение свойств элементов в четных рядах. В нечетных рядах больших периодов с увеличением заряда ядер идет заполнение электронами внешней оболочки (от 1 до 8) и свойства элементов изменяются так, как и у типических элементов.
Число электронных оболочек в атоме равно номеру периода. Атомы элементов главных подгрупп имеют на внешних оболочках число электронов, равное номеру группы. Атомы элементов побочных подгрупп содержат на внешних оболочках один или два электрона. Этим объясняется различие в свойствах элементов главной и побочной подгрупп. Номер группы указывает возможное число электронов, которые могут участвовать в образовании химических (валентных) связей (см. Молекула), поэтому такие электроны называют валентными. У элементов побочных подгрупп валентными являются не только электроны внешних оболочек, но и предпоследних. Число и строение электронных оболочек указано в прилагаемой периодической системе химических элементов.
Периодический закон Д. И. Менделеева и основанная на нем система имеют исключительно большое значение в науке и практике. Периодический закон и система явились основой для открытия новых химических элементов, точного определения их атомных весов, развития учения о строении атомов, установления геохимических законов распределения элементов в земной коре и развития современных представлений о живом веществе, состав которого и связанные с ним закономерности находятся в соответствии с периодической системой. Биологическая активность элементов и их содержание в организме также во многом определяются местом, которое они занимают в периодической системе Менделеева. Так, с увеличением порядкового номера в ряде групп возрастает токсичность элементов и уменьшается их содержание в организме. Периодический закон является ярким выражением наиболее общих диалектических законов развития природы.


